দশম শ্রেণির ৩য় সপ্তাহের রসায়ন অ্যাসাইনমেন্ট উত্তর ২০২২ প্রকাশ করা হলো। তোমরা যারা দশম শ্রেণীর শিক্ষার্থী তারা রসায়ন তৃতীয় সপ্তাহে চেয়ারম্যান 2022 এর উত্তর খুঁজছিলে। আমরা তোমাদের সেই খোঁজার অবসান ঘটালাম।
দশম শ্রেণির ৩য় সপ্তাহের রসায়ন অ্যাসাইনমেন্ট ২০২২
প্রিয় দশম শ্রেণীর শিক্ষার্থী বন্ধুরা তোমরা নিশ্চয়ই তৃতীয় সপ্তাহ অ্যাসাইনমেন্ট রসায়নের প্রশ্ন গুলো পেয়েছো। প্রশ্নগুলো না পড়ে থাকো তাহলে নিচের দেওয়া ছবি থেকে তোমরা তৃতীয় সপ্তাহে সিমেন্ট ২০২২এর প্রশ্ন গুলো পড়ে নাও।
তোমাদের রসায়ন প্রথম অধ্যায় নিশ্চয় পড়া হয়ে গেছে কারন তোমরা হচ্ছ নতুন দশম শ্রেণীর ব্যাচ। তোমাদের রসায়ন এবার প্রথম অধ্যায় থেকে দেওয়া হয়েছে। তবে ধাতব বন্ধন রয়েছে যা তোমাদের শেষের একটি অধ্যায় থেকে দেওয়া হয়েছে।
তোমরা কপারের পারমাণবিক সংখ্যা পারমাণবিক ভর এবং ইলেকট্রন বিন্যাস পড়েছ তাদের জন্য আজকের রসায়ন তৃতীয় সপ্তাহ দশম শ্রেণি অ্যাসাইনমেন্টটি খুবই সহজ হতে চলেছে।
দশম শ্রেণীর প্রিয় শিক্ষার্থী বন্ধুরা তৃতীয় সপ্তাহ রসায়ন এর নমুনা উত্তর দেখার আগে চলো আমরা প্রশ্নগুলো পড়ে নিই।

প্রশ্ন গুলো পড়ে তো নিশ্চয়ই বুঝতে পেরেছো আজকের রসায়ন তৃতীয় শক্তি খুবই সহজ। তবে তোমরা যেন ভুল না করে সেজন্য উত্তর প্রদান করব। তোমরা প্রথমে নমুনা উত্তরটি সম্পন্ন করে নিয়ে তারপর তোমাদের মূল খাতায় অর্থাৎ অ্যাসাইনমেন্ট খাতায় লেখা শুরু করবে।
১০ম শ্রেণির ৩য় সপ্তাহের রসায়ন অ্যাসাইনমেন্ট ২০২২ সমাধান
অ্যাসাইনমেন্ট শুরু
অ্যাসাইনমেন্টের শিরোনামঃ “রাসায়নিক বন্ধন গঠন, যৌগের বিভিন্ন বৈশিষ্ট্য ও ধাতুর বিদ্যুৎ পরিবাহিতা”
”ক” নং প্রশ্নের উত্তর
A ও B মৌলের মধ্যে বন্ধন গঠন ও বিদ্যুৎ পরিবাহীতাঃ উদ্দীপকে A মৌলের অবস্থান পর্যায় সারণির ১ম পর্যায় এবং গ্রুপ-১ এ। তাহলে, A মৌলটি হবে H এবং B মৌলের অবস্থান পর্যায় সারণির ২য় পর্যায় এবং গ্রুপ-১৪। তাহলে, B মৌলটি হবে C.
H ও C এর মধ্যে বন্ধন গঠনঃ H ও C এর মধ্যে সমযোজী বন্ধন বিদ্যমান। তারা পরস্পর সমযোজী বন্ধনে আবদ্ধ হয়ে CH4 উৎপন্ন করবে। সমযোজী বন্ধন হল এমন এক ধরনের রাসায়নিক বন্ধন শেয়ারের বা ভাগাভাগির মাধ্যমে আবদ্ধ থাকে। ইলেকট্রন শেয়ার করা পরমাণুদ্বয়ের মধ্যেকার আকর্ষণ ও বিকর্ষণের ফলে যে সুস্থিত ভারসাম্য বল তৈরি হয় ভাই সমযোজী বন্ধনের সৃষ্টি করে।
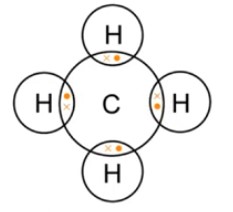
উক্ত চিত হতে দেখা যায় যে, C ও H তাদের সর্বশেষ এরা সমযোজী যৌগ।
CH4 যৌগের বিদ্যুৎ পরিবাহিতাঃ আমরা জানি, সমযোজী যৌগ গুলি সাধারণত অধাতব পরমাণুর মধ্যে ইলেকট্রন শেয়ারের মাধ্যমে পঠিত হয়। ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী যৌগ গঠিত হওয়ায়, সমযোজী যৌগের অণুডে কোন ধনাত্মক-ঋণাত্মক আধানে সৃষ্টি হয় না। এজন্য সমযোজী যৌগ গুলি সাধারণত অপোলার হয়। সমযোজী যৌগ গুলি অপোলার হওয়ার এরা তড়িৎ পরিবহন করতে পারে না।
কার্ধনের বেশিরভাগ যৌগ ইলেকট্রন শেয়ার করে সমযোজী যৌগ সৃষ্টি করে। ভাই কার্বনের যৌগ সমূহের ক্ষেত্রে দেখা যায় এরা তড়িৎ পরিবহন করে না। CH4(মিথেন) অণটি কার্বন ও হাইড্রোজেন অধাতুর পরমাপুসমূহ ইলেকট্রন শেয়ারের মাধ্যমে গঠিত হয়। অপুটিতে ধনাত্মক-ঋণাত্মক আধান গঠিত না হওয়ার মিখেন অনুটি বিদ্যুৎ পরিবহন করে না।
(ধা নং প্রশ্নের উত্তর)
C ও D মৌলের মধ্যে বন্ধন গঠন ও বিদ্যুৎ পরিবাহীতাঃ উদ্দীপকে C মৌলের অবস্থান পর্যায় সারণির ২য় পর্যায় এবং গ্রুপ-১৬ এ। তাহলে, C মৌলটি হবে O. এবং D মৌলের অবস্থান পর্যায় সারণির ৪র্থ পর্যায় এবং গ্রুপ-১। তাহলে, D মৌলটি হবে K.
O ও K এর মধ্যে বন্ধন গঠনঃ O ও K এর মধ্যে আরনিক বন্ধন বিদ্যমান। তারা পরস্পর ইলেকট্রন আদান প্রদানের মাধ্যমে আয়নিক বন্ধনে আবদ্ধ হয়ে K2O উৎপন্ন করবে।
আয়নীয় বন্ড বা ভড়িৎযোজী বন্ধন হল এক প্রকার রাসায়নিক বন্ধন, যা বিপরীত আধানযুক্ত আয়নসমূহের মধ্যে স্থির-ভাড়িৎ আকর্ষণ সৃষ্টি করে। এছাড়া এই বন্ধন আয়নীয় যৌগে ক্রিয়াশীল একটি প্রাথমিক বল। এককথায়, পূর্ণ যোজ্যতা কক্ষ লাভের জন্য ধাতু থেকে অধাতুর দিকে ইলেক্টনের সরণই হল আয়নীয় বন্ধন।
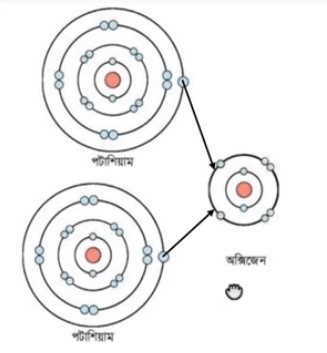
K2O যৌগের গলনাংক ও স্ফুটনাংকঃ
আমরা জানি, আয়নিক যৌগের অপুতে পরমানু সমহের মধ্যে বিদ্যামান বন্ধন শক্তি, সমযোজী যৌগের অপুতে বিদ্যামান পরমাণুসমূহের মধ্যকার বন্ধন শক্তি অপেক্ষা বেশি থাকে। আবার আয়নিক যৌগের পরমাণু সমূহ ধনাত্মক-ঋণাত্মক চার্জিত থাকে। এই ধনাত্মক-ঋণাত্মক আধান অনু গঠনের সময় ত্রিমাত্রিক ভাবে সুবিন্যান্ত হয়ে জ্যামিতিক কাঠামো গঠন করে। এতে করে আরনিক যৌগের একটি ক্যাটায়ন নির্দিষ্ট সংখ্যক আ্যানায়ন দ্বারা এবং আয়নিক যৌগের একটি আ্যানায়ন নির্দিষ্ট সংখ্যক ক্যাটায়ন দ্বারা পরিবেষ্টিত থাকে। এতে আয়নিক যৌসের অপুতে আন্তঃআশবিক আকর্ষণ বল অনেক বেশি হয়। ফলে আয়নিক যৌগের অণু কে ভাঙতে অনেক বেশি তাপ শক্তির প্রয়োজন হয়। তাই আয়নিক যৌগের গললাঙ্ক ও স্ফুটনান্ক অনেক বেশি হয়।
K2O আয়নিক বন্ধন দ্বারা তৈরি। তাই তারা আয়নিক যৌগ। তাই K2O এর গলনাংক ও স্ফুটনাংক অনেক বেশি।
শুধু K2O যৌগের গলনাংক হলো 35০০ থেকে 740০ পর্যন্ত।
(গ নং প্রশ্নের উত্তর)
“খ” হতে পাই, D মৌলটি হলো K। K এর একাধিক পরমাপুর মধ্যে ধাতব বন্ধন যিদ্যমান।
K বিদ্যুৎ পরিবাহিতা দেখানো হলোঃ
একটি ধাতু অপর একটি অধাত্র মধ্যে আয়নিক বন্ধন এবং দুটি অধাতুর মধ্যে সমযোজী বন্ধন গঠিত হয়। কিন্ত দুট ধাতব পরমাণু কাছাকাছি এলে তাদের মধ্যে যে বন্ধন গঠিত হয় তাকে ধাতব বন্ধন বলে। ধাতু সমহ যে ধরনের বন্ধনের মাধ্যমে পরম্পরের সাথে যুক্ত থাকে তা ই ধাতব বন্ধন। এই সঙঞ্চারণশীল ইলেকট্রন এবং ধনাক্সক চার্জ যুক্ত ধাতব আয়নের মধ্যে হয়ে থাকে। এই বিশেষ ধরনের বন্ধনের কারণেই ধাতু ভাপ এবং বিদ্যুৎ পরিবহন করে।
এই বন্ধন সঙ্চারপশীল ইলেকট্রন এবং ধনাল্সক চার্জ যুক্ত ধাতব আয়নের মধ্যে হয়ে খাকে। ধাতব বন্ধন ধাতুর অনেকগুলো ভৌত ধর্ম যেমন: যান্ত্রিক শক্তি. নমনীয়তা, তাপ এবং বৈদ্যতিক রোধ এবং পরিবাহিতা, অস্বচ্ছতা এবং দীস্তির জন্য দায়ী।
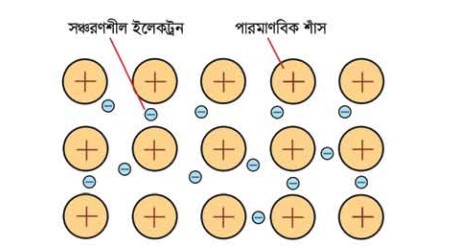
পটাশিয়াম একটি ধাতব মৌল হওয়ায় এর দ্বারা গঠিত বন্ধন হবে ধাতব বন্ধন। ইলেকট্রন বিন্যাস অনুসারে, এর সর্বশেষ স্তরে একটি মুফ ইলেকট্রন বিদ্যমান থাকায় ইলেকট্রনটি সঞ্চারণশীল হয় এবং পারমাণবিক শাঁসের মধ্যে চলাচল করে বিদ্যুৎ পরিবহণ করে। তাই বলা যায় যে. পটাশিয়াম (K) বিদ্যুৎ পরিষহণ করে।
অ্যাসাইনমেন্ট শেষ
আরো পড়ুনঃ
- সকল শ্রেণির সকল অ্যাসাইনমেন্ট দেখুন
- ৬ষ্ঠ শ্রেণির ৩য় সপ্তাহের বাংলা অ্যাসাইনমেন্ট উত্তর ২০২২
- ৭ম শ্রেণির ৩য় সপ্তাহের বাংলা অ্যাসাইনমেন্ট উত্তর ২০২২
- ৮ম শ্রেণির ৩য় সপ্তাহের বাংলা অ্যাসাইনমেন্ট উত্তর ২০২২
- ৯ম শ্রেণির ৩য় সপ্তাহের বাংলা অ্যাসাইনমেন্ট উত্তর ২০২২
- ১০ম শ্রেণির ৩য় সপ্তাহের বাংলা অ্যাসাইনমেন্ট উত্তর ২০২২
- ষষ্ঠ শ্রেণির ৩য় সপ্তাহের বিজ্ঞান অ্যাসাইনমেন্ট উত্তর ২০২২
- ৭ম শ্রেণির ৩য় সপ্তাহের বিজ্ঞান অ্যাসাইনমেন্ট উত্তর ২০২২
- ৮ম শ্রেণির ৩য় সপ্তাহের বিজ্ঞান অ্যাসাইনমেন্ট উত্তর ২০২২
- ৯ম শ্রেণির ৩য় সপ্তাহের ব্যসসায় উদ্যোগ অ্যাসাইনমেন্ট উত্তর ২০২২
- ১০ম শ্রেণির ৩য় সপ্তাহের ব্যসসায় উদ্যোগ অ্যাসাইনমেন্ট উত্তর ২০২২
- ৯ম শ্রেণির ৩য় সপ্তাহের রসায়ন অ্যাসাইনমেন্ট উত্তর ২০২২
- ১০ম শ্রেণির ৩য় সপ্তাহের রসায়ন অ্যাসাইনমেন্ট উত্তর ২০২২
- ৯ম শ্রেণির ৩য় সপ্তাহের ভূগোল ও পরিবেশ অ্যাসাইনমেন্ট উত্তর ২০২২
- ১০ম শ্রেণির ৩য় সপ্তাহের ভূগোল ও পরিবেশ অ্যাসাইনমেন্ট উত্তর ২০২২



