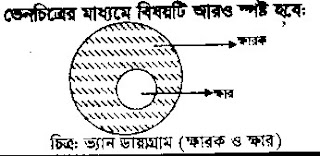
ক্ষারক ও ক্ষার চেনার সহজ উপায়
অনেকের ক্ষার এবং ক্ষারক সম্মন্ধে সঠিক ধারণা নেই। ক্ষার এবং ক্ষারকের মধ্যে পার্থক্য কোথায়? ক্ষার এবং ক্ষারকের গঠন দেখতে একই রকম হলেও তাদের মধ্যে কিন্তু বিস্তর পার্থক্য রয়েছে। নিচের বিষয়গুলো বুঝতে পারলে এ সম্মন্ধে আর কোন সমস্যা থাকবেনা বলে আশা করা যায়।
ক্ষারক চেনার উপায়ঃ
i) ক্ষারক হলো ধাতব অক্ষাইড (O²⁻) বা হাইড্রোক্ষাইড (OH⁻)
অর্থাৎ ধাতু + অক্সাইড = ক্ষারক
Na+O²⁻ = Na₂O
ধাতু + হাইড্রোক্সাইড = ক্ষারক
K + OH⁻ = KOH
ii) ক্ষারক পদার্থ এসিডকে প্রশমিত করে লবণ ও পানি উৎপন্ন করে।
যেমনঃ KOH +HCl → KCl +H₂O
ক্ষার এসিড লবণ পানি
iii) ক্ষারক পদার্থ পানিতে দ্রবীভূত হতেও পারে আবার দ্রবীভূত নাও হতে পারে।
অর্থাৎ যে সব ধাতব অক্সাইড বা হাইড্রোক্সাইড পানিতে দ্রবণীয় তারা ক্ষারক এবং পানিতে অদ্রবণীয় তারাও ক্ষারক।
অর্থাৎ ক্ষারক = পানিতে দ্রবনীয় অথবা অদ্রবনীয় অক্সাইড বা হাইড্রোক্সাইড।
যেমনঃ NaOH , KOH প্রভৃতি যৌগ পানিতে দ্রবীভূত হয়। সুতরাং এরা ক্ষারক।
আবার (OH)₃ , CuO প্রভৃতি যৌগ পানিতে দ্রবনীয় হয়না তবুও এরা ক্ষারক।
iv) ক্ষারকের pH এর মান 7 এর বেশী হবে।
v) ক্ষারক পদার্থের শেষে O²⁻ (অক্সাইড) বা OH⁻ (হাইড্রোক্সাইড) মূলক অবশ্যই থাকবে।
vi) ক্ষারকগুলো জলীয় দ্রবণে OH আয়ন উৎপন্ন করবে।
vii) এটি লাল লিটমাসকে নীল করে।
ক্ষারকের উদাহরণঃ
- পানিতে দ্রবণীয় ক্ষারকসমূহঃ NaOH, KOH, LiOH, Ca(OH)₂, Ba(OH)₂
- পানিতে অদ্রবণীয় ক্ষারকসমূহঃ Al(OH)₃, CuO, FeO, Fe(OH)₂, NH₃
মনে রাখাঃ NH₄OH একটি ক্ষারক যদিও এটি ধাতব হাইড্রোক্সাইড নয়। এটি ব্যতিক্রম।
ক্ষার চেনার সহজ উপায়ঃ
i) ক্ষার হলো ধাতব অক্সাইড ধাতব অক্ষাইড (O²⁻) বা হাইড্রোক্ষাইড (OH⁻) বিশিষ্ট যৌগ।
যেমানঃ Ca(OH)₂, KOH, CaO,
ii) ক্ষার পদার্থ এসিডকে প্রশমিত করে লবণ ও পানি উৎপন্ন করে।
iii) ক্ষার অবশ্যই পানিতে দ্রবীভূত হবে। যদি পানিতে দ্রবীভূত না হয় তাহলে সেটি ক্ষার হবেনা।
∴ ক্ষার= পানিতে দ্রবীভূত ধাতব অক্সাইড/হাইড্রোক্সাইড
NaOH পানিতে দ্রবীভূত হয়ে বলে এটি ক্ষার বা ক্ষারক কিন্তু Al(OH)₃ পানিতে দ্রবীভূত হয় না তাই এটি শুধু ক্ষারক, ক্ষার নয়।
iv) ক্ষারের pH এর মান 7 এর বেশী হবে।
v) ক্ষার পদার্থের শেষে O²⁻ (অক্সাইড) বা OH⁻ (হাইড্রোক্সাইড) মূলক অবশ্যই থাকবে।
NaOH CaO
↓ ↓
OH⁻ O²⁻ যুক্ত আছে
vii) ক্ষারগুলো জলীয় দ্রবণে OH আয়ন উৎপন্ন করবে।
ক্ষারের উদাহরণঃ
NaOH, KOH, LiOH, Ca(OH)₂, Ba(OH)₂, Cs(OH)2, NH₄OH, ইত্যাদি
সকল ক্ষারই ক্ষারক কিন্তু সকল ক্ষারক ক্ষার নয়।
মনে রাখুনঃ- ক্ষারক শব্দটির মধ্যে ক্ষার আছে কিন্তু ক্ষার শব্দটিকে ’ক’ নাই অর্থাৎ ক্ষারক নাই।
যেমনঃ NaOH = ক্ষার + ক্ষারক
Al(OH)₃ = শুধু ক্ষারক
ক্ষারক
↙ ↘
পানিতে পানিতে
অদ্রবণীয় দ্রবণীয় (ক্ষার)
লেখাটি ভালো লাগলে শেয়ার করুন।