টেকনিক্যাল নবম শ্রেণি রসায়ন অ্যাসাইনমেন্ট ২ technical class 9 chemistry assignment
শিরোনামঃ ২নং রসায়ন অ্যাসাইনমেন্ট
- ৩য় সপ্তাহের (৯ম) নবম শ্রেণির কৃষি শিক্ষা এসাইনমেন্ট উত্তর ২০২১।
- নবম শ্রেণির জীববিজ্ঞান অ্যাসাইনমেন্ট উত্তর ২য় সপ্তাহ ২০২১
- নবম (৯ম) শ্রেণীর অ্যাসাইনমেন্ট বাংলা ১ম সপ্তাহ ২০২১ প্রশ্ন ও সমাধান
- নবম শ্রেণীর বাংলাদেশ ও বিশ্বপরিচয় অ্যাসাইনমেন্ট ১ম সপ্তাহ ২০২১ প্রশ্ন ও সমাধান
- ৬ষ্ঠ শ্রেণির অ্যাসাইনমেন্ট ইংরেজি উওর ২য় সপ্তাহ ২০২১
- ৯ম শ্রেণির ফিন্যন্স ও ব্যাংকিং অ্যাসাইনমেন্ট ২য় সপ্তাহ ২০২১
টেকনিকাল নবম শ্রেণি রসায়ন অ্যাসাইনমেন্ট প্রশ্নগুলো দেখুন
রসায়ন শিক্ষক তোমাকে 200ml আয়তনিক ফ্লাক্সে 0.5M সোডিয়াম কার্বনেট দ্রবণ তৈরি করতে বললেন। এ তথ্যের আলোকে নিম্নের প্রশ্নগুলোর উত্তর দাও।
১) মোল কাকে বলে?
২) দ্রবণটি তৈরি করতে কী কী যন্ত্রপাতির প্রয়োজন।
৩) প্রদত্ত যৌগটির শতকরা সংযুক্তি নির্ণয় কর।
৪) দ্রবণটি তুমি কিভাবে তৈরী করবে তার ধারাবাহিক পদ্ধতি বর্ণনা কর।
১নং প্রশ্নের উত্তর
মোলঃ রাসায়নিক পদার্থের (পরমাণুর ক্ষেত্রে) পারমাণবিক ভর অথবা (অণুর ক্ষেত্রে) আণবিক ভরকে গ্রাম এককে প্রকাশ করলে যে পরিমাণ পাওয়া যায় তাকে এঁ পদার্থের এক মোল বলা হয়।
২নং প্রশ্নের উত্তর
দ্রবণটি তৈরি করতে প্রয়োজনীয় যন্ত্রপাতিঃ ২০০মিলিলিটার আয়তনিক ফ্লাক্স, ফানেল, ওজন, বোতল, রাসায়নিক নিক্তি, ওয়াশ বোতল।
৩নং প্রশ্নের উত্তর
প্রদত্ত যৌগটি হলো সোডিয়াম কার্বনেট Na₂(CO₃) নিচে সোডিয়াম কার্বনেটের শতকরা সংযুক্তি বের করে দেখানো হলো।
সোডিয়াম কার্বনেট Na₂(CO₃) এর আনবিক ভর = 23×2+12×1+16×3
= 46+12+48
= 106
Na এর শতকরা সংযুক্তি = (23×2×100) ÷ 106
= 43.39%
C এর শতকরা সংযুক্তি = (12×1×100) ÷ 106
= 11.32%
O এর শতকরা সংযুক্তি = (16×3×100) ÷ 106
= 45.28%
৪ নং প্রশ্নের উত্তর
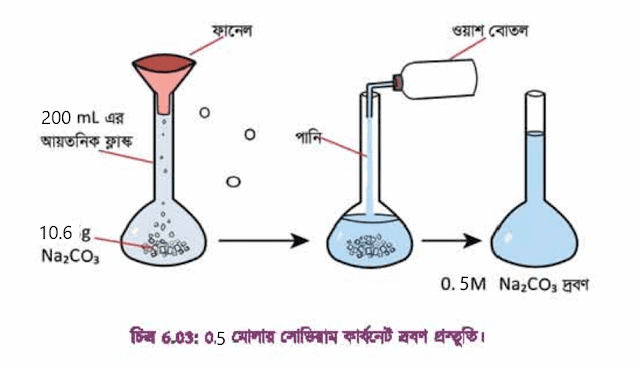
200 মিলি আয়তনিক ফ্লাক্সে 0.5 মোলার সোডিয়াম কার্বনেট দ্রবণ প্রস্তুতি।
মূলনীতি: সোডিয়াম কার্বনেট Na₂(CO₃) একটি প্রাইমারি স্ট্যান্ডার্ড পদার্থ। কারণ সোডিয়াম কার্বনেটকে বিশুদ্ধ অবস্থায় পাওয়া যায়, শুষ্ক অবস্থায় পাওয়া যায়, রাসায়নিক নিস্তিতে সরাসরি ওজন করা যায়, সোডিয়াম কার্বনেট দ্রবণের ঘনমাত্রা তৈরি করে থাকলে ঐ ঘনমাত্রা দীর্ঘদিন কোনো পরিবর্তন হয় না। একটি 200 মিলি আয়তনিক ফ্লাক্সে 0.5 মোলার সোডিয়াম কার্বনেট দ্রবণ তৈরি করার জন্য নিচের হিসাৰ প্রয়োজন।
এখানে, V = 200 মিলি , S= 0.5 মোলার, M= 23×2+12×1+16×3 =106
W =?
আমরা জানি, W = SVM/1000
= (0.5×200×106)/1000
∴W = 10.6 গ্রাম
একটি আয়তনিক ফ্লাক্সে 10.6 গ্রাম সোডিয়াম কার্বনেট মেপে নিয়ে তার মধ্যে পানি যোগ করে দ্রবণের আয়তন 200 মিলিলিটার করলে 0.5 মোলার সোডিয়াম কার্বনেট ভ্রবণ প্রস্তুত হয়ে হাবে। কিন্তু এই নির্দিষ্ট্য ঘনমাত্রার (মোলারিটির) দ্রবণ তৈরি করা অত্যন্ত কষ্টসাধ্য। কারণ সঠিকভাবে 10.6 গ্রাম সোডিয়াম কার্বনেট মেপে নেওয়া অত্যন্ত কঠিন। অতএব, 0.5 মোলার ঘনমাত্রার কাছাকাছি কোনো ঘনমাত্রার দ্রবণ তৈরি করা হয়।
দ্রবণটি তৈরি করতে প্রয়োজনীয় যন্ত্রপাতিঃ
২০০মিলিলিটার আয়তনিক ফ্লাক্স, ফানেল, ওজন, বোতল, রাসায়নিক নিক্তি, ওয়াশ বোতল।
কার্যপদ্ধতিঃ
১) একটি পরিষ্কার ২০০ মিলি আয়তনিক ফ্লাক্সের মুখে একটি পরিষ্কার ফানেল রাখা হলো।
২) রাসায়নিক নিক্তির সাহায্যে ১টি শুষ্ক ওজন বোতলের ওজন নেওয়া হলো।
৩) এবার ওজন বোতলে সোডিয়াম কার্বনেট এমনভাবে দেওয়া হলো যেন সোডিয়াম কার্বনেটসহ ওজন বোতলের ওজন 10.6 গ্রাম বেশি হয়।
৪) ওজন বোতলের সোডিয়াম কার্বনেট ফানেলের মধ্য দিয়ে আয়তনিক ফ্লাক্সে ঢালা হলো ।
৫) ওয়াশ বোতল থেকে পাতিত পানি ফানেলের মাধ্যমে আয়তনিক ফ্লাক্সে আস্তে আন্তে যোগ করা হলো। অর্ধেক পানি ঢালার পর আয়তনিক ফ্লাক্ষের মুখের ছিপি আটকিন়ে আয়তনিক ফ্লাক্স ঝাঁকিয়ে সোডিয়াম কার্বনেটকে সম্পূর্ণভাবে ভ্রবীভূত করা হলো। এরপর আরো পানি যোগ করে আয়তনিক ফ্লাস্কের 200. দাগ পর্যন্ত পানি দ্বারা পূর্ণ করা হলো।
সতর্কতাঃ
১) শুক্ষ ও বিশুদ্ধ সোডিয়াম কার্বনেট নেওয়া ।
২) শুষ্ক ওজন বোতল নেওয়া ।
৩) বিশুদ্ধ পানি অর্থাৎ পাতিত পানি আয়তনিক ফ্লাস্কে যোগ করা।
যে কোনো অ্যাসাইনমেন্টের জন্য নিচে কমেন্ট করুন।