নবম দশম/এসএসসি রসায়ন সপ্তম অধ্যায় রাসায়নিক বিক্রিয়া এর পাঠ সম্পর্কিত গুরুত্বপূর্ণ বিষয়াদি,জ্ঞানমূলক প্রশ্ন ও উত্তর ও অনুধাবনমূলক প্রশ্ন ও উত্তর নিচে দেওয়া হলো।
এসএসসি রসায়ন সপ্তম অধ্যায় রাসায়নিক বিক্রিয়া
রসায়ন সপ্তম অধ্যায় পাঠ সম্পর্কিত গুরুত্বপূর্ণ বিষয়াদি
⇒ পদার্থের পরিবর্তন : যে পরিবর্তন থেকে পদার্থের বাহ্যিক অবস্থা এবং মূল গঠন বা অণুর গঠনের সাধারণ পরিচয় পাওয়া যায় তাকে পদার্থের পরিবর্তন বলে।
⇒ ভৌত পরিবর্তন : যে পরিবর্তনে পদার্থের মূল গঠনের কোনো পরিবর্তন ঘটে না অর্থাৎ কোনো নতুন পদার্থ উৎপন্ন হয় না, শুধু পদার্থের বাহ্যিক বা ভৌত অবস্থার রূপান্তর ঘটে, সেই পরিবর্তনকে ভৌত পরিবর্তন বলে। ভৌত পরিবর্তন অস্থায়ী। এই পরিবর্তনে পদার্থের অণুর গঠনের কোনো পরিবর্তন হয় না। বরফের গলন, পানির স্ফুটন, লোহার চুম্বকে পরিবর্তন, মোমের গলন ইত্যাদি ভৌত পরিবর্তনের উদাহরণ।
⇒ রাসায়নিক পরিবর্তন : যে পরিবর্তনে পদার্থের মূল গঠনের পরিবর্তন ঘটে এবং পদার্থটি এক বা একাধিক ভিন্ন ধর্মবিশিষ্ট নতুন পদার্থে পরিণত হয়, সেই পরিবর্তনকে রাসায়নিক পরিবর্তন বলে। রাসায়নিক পরিবর্তন স্থায়ী। এই পরিবর্তনে পদার্থের অণুর গঠনে আমূল পরিবর্তন ঘটে। লোহায় মরিচা পড়া, মোমবাতির দহন, দুধ থেকে দই প্রস্তুত, চাল থেকে ভাত তৈরি ইত্যাদি রাসায়নিক পরিবর্তনের উদাহরণ।
⇒ একমুখী বিক্রিয়া : যে বিক্রিয়ায় সকল বিক্রিয়ক পদার্থ একটি নির্দিষ্ট সময় পরে উৎপাদে পরিণত হয় তাকে একমুখী বিক্রিয়া বলে। একমুখী বিক্রিয়া শুধু সম্মুখদিকে অগ্রসর হয়। এ বিক্রিয়ায় বিক্রিয়ক ও উৎপাদের মধ্যে একমুখী (→) চিহ্ন ব্যবহার করা হয়। যেমন : পটাসিয়াম ক্লোরেটকে উত্তপ্ত করলে এটি বিয়োজিত হয়ে পটাসিয়াম ক্লোরাইড ও অক্সিজেন উৎপন্ন হয়। বিপরীতভাবে, পটাসিয়াম ক্লোরাইড ও অক্সিজেনের মধ্যে কোনো বিক্রিয়া ঘটে না। সুতরাং, এটি একটি একমুখী বিক্রিয়া।
2KClO3 → 2KCl + 3O2
⇒ উভমুখী বিক্রিয়া : যদি কোনো বিক্রিয়া একসাথে সম্মুখদিক ও বিপরীত দিক থেকে সংঘটিত হয়, ওই বিক্রিয়াকে উভমুখী বিক্রিয়া বলে। উভমুখী বিক্রিয়ায় বিক্রিয়কসমূহ কখনোই সম্পূর্ণরূপে উৎপাদে পরিণত হয় না। নির্দিষ্ট তাপমাত্রা ও চাপে বিক্রিয়কের একটি অংশমাত্র উৎপাদে পরিণত হয়। উভমুখী বিক্রিয়ায় বিক্রিয়ক এবং উৎপাদের মধ্যে উভমুখী তীর চিহ্ন (⇔ ) ব্যবহার করা হয়। যেমন : হাইড্রোজেন ও আয়োডিনকে একটি আবদ্ধ পাত্রে নিয়ে উত্তপ্ত করা হলে কিছুটা বিক্রিয়ক হাইড্রোজেন আয়োডাইড উৎপন্ন করে। বিক্রিয়াটি নিম্নরূপে ঘটে-
H2 + I2 ⇔ 2HI
⇒ তাপ উৎপাদী বিক্রিয়া : যে রাসায়নিক বিক্রিয়ায় তাপ উৎপন্ন হয় তাকে তাপ উৎপাদী বিক্রিয়া বলে। যেমন :
হাইড্রোজেন ও নাইট্রোজেনের বিক্রিয়ায় অ্যামোনিয়া উৎপন্ন হয়। এতে তাপ উৎপন্ন হয়।
N2 + 3H2 (Fe প্রভাবক)⇔ 2NH3 + 92 kJ
⇒ তাপহারী বিক্রিয়া : যে রাসায়নিক বিক্রিয়ায় তাপ শোষিত বা গৃহীত হয় তাকে তাপহারী বা তাপগ্রাহী বা তাপ শোষক বিক্রিয়া বলে। যেমন :
নাইট্রোজেন এবং অক্সিজেনের সংযোগে নাইট্রিক অক্সাইড গ্যাস উৎপন্ন হয় এবং তাপ শোষিত হয়।
N2 + O2 = 2NO – 180 kJ
⇒ রেডক্স বিক্রিয়া : রেডক্স অর্থ জারণ-বিজারণ। যে বিক্রিয়া ইলেকট্রন স্থানান্তরের মাধ্যমে সংঘটিত হয় তাকে জারণ-বিজারণ বিক্রিয়া বা রেডক্স বিক্রিয়া বলে। এতে বিক্রিয়কের জারণ সংখ্যার পরিবর্তন হয়।
⇒ জারণ সংখ্যা : যৌগ গঠনের সময় কোনো মৌল যত সংখ্যক ইলেকট্রন বর্জন করে ধনাত্মক আয়ন উৎপন্ন করে অথবা যত সংখ্যক ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়ন উৎপন্ন করে তাকে মৌলের জারণ সংখ্যা বলে। নিরপেক্ষ বা মুক্ত মৌলের জারণ সংখ্যা শূন্য (০) ধরা হয়। ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে পরিণত হলে মৌলের জারণ সংখ্যাকে ঋণাত্মক জারণ সংখ্যা এবং ইলেকট্রন বর্জন করে ধনাত্মক আয়নে পরিণত হলে মৌলের জারণ সংখ্যাকে ধনাত্মক জারণ সংখ্যা বলে।
⇒ জারক ও বিজারক : জারণ-বিজারণ বিক্রিয়ার সময় যে বিক্রিয়ক ইলেকট্রন গ্রহণ করে তাকে জারক এবং যে বিক্রিয়ক ইলেকট্রন বর্জন করে তাকে বিজারক বলে। O2, H2O2, O3, HNO3, গাঢ় H2SO4, হ্যালোজেন (F2, Cl2, Br2, I2), MnO2, KMnO4, K2Cr2O7, KClO3 প্রভৃতি জারক পদার্থ। H2, H2S, C, CO, SO2, Na, Mg, SnCl2, HI, HBr, NH3, HNO2 প্রভৃতি বিজারক পদার্থ।
⇒ জারণ ও বিজারণ একই সঙ্গে ঘটে : রাসায়নিক বিক্রিয়ায় জারণ ও বিজারণ ক্রিয়া একই সঙ্গে ঘটে। কারণ জারণ ক্রিয়ায় জারক পদার্থ বিজারিত হয়। আবার, বিজারণ ক্রিয়ায় বিজারক পদার্থ নিজে জারিত হয়। সুতরাং, জারণ ক্রিয়া ঘটলেই বিজারণ ক্রিয়াও ঘটবে। জারণ ও বিজারণ বিক্রিয়াকে একই সঙ্গে রেডক্স (Redox) বিক্রিয়া বলা হয়।
⇒ সংযোজন বিক্রিয়া : দুই বা ততোধিক যৌগ বা মৌল যুক্ত হয়ে নতুন যৌগ উৎপন্ন হওয়ার প্রক্রিয়ার নাম সংযোজন বিক্রিয়া। যেমন :
2FeCl2 (aq) + Cl2(g) ® 2FeCl3 (aq); H2(g) + Cl2 (g) ® 2HCl (g)
⇒ বিযোজন বিক্রিয়া : কোনো যৌগকে ভেঙে একাধিক যৌগ বা মৌলে পরিণত করার প্রক্রিয়ার নাম বিযোজন বিক্রিয়া। যেমন :
2FeCl2 (aq) + Cl2(g) ® 2FeCl3 (aq); H2(g) + Cl2 (g) ® 2HCl (g)
⇒ প্রতিস্থাপন বিক্রিয়া : কোনো যৌগের একটি মৌল বা যৌMgূলককে অপর কোনো মৌল বা যৌMgূলক দ্বারা প্রতিস্থাপন করে নতুন যৌগ উৎপন্ন করার প্রক্রিয়ার নাম প্রতিস্থাপন বিক্রিয়া। যেমন :
Zn
Zn (s) + H2SO4 (aq) ® ZnSO4 (aq) + H2 (g); 2Na (s) + CuSO4(aq) ®Na2SO4(aq) + Cu(s)
⇒ দহন বিক্রিয়া : কোনো মৌলকে বা যৌগকে বায়ুর অক্সিজেনের উপস্থিতিতে পুড়িয়ে তার উপাদান মৌলের অক্সাইডে পরিণত করার প্রক্রিয়াকে দহন বিক্রিয়া বলে। যেমন :
CH4(g) + 2O2(g) ® CO2(g) + 2H2O(g); C(s) + O2(g) ® CO2(g)
2H2(g) + O2(g) → 2H2O(g)
⇒ নন-রেডক্স বিক্রিয়া : এক বা একাধিক বিক্রিয়ক থেকে নতুন যৌগ উৎপন্ন হওয়ার সময় বিক্রিয়কে বিদ্যমান মৌলসমূহের মধ্যে ইলেকট্রন আদান-প্রদান না হলে বিক্রিয়াকে নন-রেডক্স বিক্রিয়া বলে। প্রশমন বিক্রিয়া ও অধঃক্ষেপণ বিক্রিয়া নন-রেডক্স বিক্রিয়া।
⇒ প্রশমন বিক্রিয়া : জলীয় দ্রবণে এসিড ও ক্ষার বিক্রিয়া করে লবণ ও পানি উৎপন্ন করার বিক্রিয়াকে প্রশমন বিক্রিয়া বলে। প্রশমন বিক্রিয়া সম্পন্ন হলে pH-এর মান 7 হয়। যেমন :
HCl(aq) + NaOH(aq) → NaCl(aq) + H2(l)
⇒ অধঃক্ষেপণ বিক্রিয়া : যে বিক্রিয়ায় উৎপন্ন যৌগ অধঃক্ষেপ হিসেবে পাত্রের তলদেশে জমা হয় তাকে অধঃক্ষেপণ বিক্রিয়া বলে। অধঃক্ষেপকে প্রকাশ করার জন্য উৎপাদের সামনে চিহ্ন ব্যবহার করা হয়। যেমন :
NaCl(aq) + AgNO3(aq) → NaNO3(aq) + AgCl(s)
⇒ আর্দ্রবিশ্লেষণ বা পানি বিশ্লেষণ বিক্রিয়া : পানির অণুতে ধনাত্মক হাইড্রোজেন আয়ন (H+) ও ঋণাত্মক হাইড্রোক্সিল আয়ন (OH-) থাকে। কোনো যৌগের দুই অংশ পানির বিপরীত আধানবিশিষ্ট দুই অংশের সাথে যুক্ত হয়ে নতুন যৌগ উৎপন্ন করে। এই বিক্রিয়াকে আর্দ্রবিশ্লেষণ বিক্রিয়া বলে। যেমন :
AlCl3(s) + 3H2O(l) → Al(OH)3(s) + 3HCl(aq)
SiCl4 + 4H2O → Si(OH)4 + 4HCl
⇒ পানিযোজন বিক্রিয়া : আয়নিক যৌগ কেলাস গঠনের সময় এক বা একাধিক সংখ্যক পানির অণুর সাথে যুক্ত হয়। এই বিক্রিয়াকে পানিযোজন বিক্রিয়া বলে। যেমন :
CaCl2 + 6H2O → CaCl2.6H2O
MgCl2 + 7H2O → MgCl2.7H2O
CuSO4 + 5H2O → CuSO4.5H2O
⇒ সমাণুকরণ বিক্রিয়া : একই আণবিক সংকেতবিশিষ্ট দুটি যৌগের ধর্ম ভিন্ন হলে তাদেরকে পরস্পরের সমাণু বলে। যেমন : C2H6O আণবিক সংকেত বিশিষ্ট দুটি যৌগ CH3CH2OH (ইথানল) ও CH3OCH3 (ডাই মিথাইল ইথার)
⇒ পলিমারকরণ বিক্রিয়া : যে বিক্রিয়ায় অসংখ্য মনোমার থেকে পলিমার উৎপন্ন হয় তাকে পলিমারকরণ বিক্রিয়া বলে। যেমন : উচ্চতাপ ও চাপের প্রভাবে ভিনাইল ক্লোরাইড (CH2 = CHCl)-এর অসংখ্য অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ আণবিক ভরবিশিষ্ট নতুন যৌগ পলিভিনাইল ক্লোরাইড (PVC) গঠন করে।
nH2C = CHCl(g) উচ্চ তাপ ও চাপ→ [ – CH2 – CHCl – ]n(s)
⇒ ইলেকট্রোপ্লেটিং : তড়িৎ বিশ্লেষণ প্রক্রিয়ায় লোহা, তামা, পিতল প্রভৃতি ধাতু বা ধাতু সংকরের তৈরি দ্রব্যের ওপর নিকেল, জিংক, সিলভার, গোল্ড, ক্রোমিয়াম প্রভৃতি ধাতুর প্রলেপ দেয়াকে ইলেকট্রোপ্লেটিং বলা হয়। কোনো কোনো ধাতুর তৈরি জিনিসপত্রকে জলবায়ু এবং বায়ুর অক্সিজেনের প্রকোপ থেকে রক্ষা করা এবং দেখতে সুন্দর ও আকর্ষণীয় করে তোলাই ইলেকট্রোপ্লেটিং-এর উদ্দেশ্য।
⇒ বিক্রিয়ার গতিবেগ বা বিক্রিয়ার হার : একক সময়ে একটি বিক্রিয়ার বিক্রিয়কসমূহের ঘনমাত্রা কতটুকু হ্রাস পায় বা উৎপন্ন পদার্থের ঘনমাত্রা কতটুকু বৃদ্ধি পায় তাকে বিক্রিয়ার হার বা গতি বলে।
⇒ বিক্রিয়ার বেগ বা গতির ওপর তাপমাত্রা, ঘনমাত্রা ও প্রভাবকের প্রভাব : রাসায়নিক বিক্রিয়ার গতিবেগ কয়েকটি নিয়ামকের ওপর নির্ভরশীল। তন্মধ্যে তাপমাত্রা, বিক্রিয়কের ঘনমাত্রা ও প্রভাবকের উপস্থিতি বিশেষভাবে গুরুত্বপূর্ণ। ঘনমাত্রা বাড়ালে বিক্রিয়ার গতিবেগ বাড়ে। প্রভাবকের উপস্থিতিতে বিক্রিয়ার গতিবেগ বাড়ে বা কমে।
⇒ রাসায়নিক সাম্যাবস্থা : যে অবস্থায় কোনো উভমুখী বিক্রিয়ার সম্মুখ বিক্রিয়ার গতিবেগ বিপরীতমুখী বিক্রিয়ার গতিবেগের সমান হয় সে অবস্থাকে রাসায়নিক সাম্যাবস্থা বলে। রাসায়নিক সাম্যাবস্থায় তাপমাত্রা, চাপ এবং অংশগ্রহণকারী পদার্থের দৃশ্যমান ধর্মগুলো স্থির থাকে। বিক্রিয়ার উভমুখিতার ফলেই সাম্যাবস্থার উদ্ভব ঘটে। একটি উভমুখী বিক্রিয়ার শুরুতে সম্মুখ বিক্রিয়ার বেগ সবচেয়ে বেশি থাকবে এবং বিপরীত বিক্রিয়ার বেগ কম থাকবে। সময়ের সঙ্গে বিক্রিয়কের পরিমাণ কমতে থাকবে ও উৎপাদের পরিমাণ বাড়তে থাকবে।
⇒ লা-শাতেলিয়ার নীতি : বিখ্যাত ফরাসি বিজ্ঞানী লা-শাতেলিয়ে 1884 সালে উভমুখী বিক্রিয়ার সাম্যাবস্থার ওপর বিভিন্ন নিয়ামকের প্রভাব সম্পর্কিত একটি নীতি উপস্থাপন করেন যা লা-শাতেলিয়ার নীতি নামে পরিচিত। নীতিটি হলো-
“যেসব নিয়ামক যেমন : তাপমাত্রা, চাপ, ঘনমাত্রা ইত্যাদির ওপর কোনো উভমুখী বিক্রিয়ার সাম্যাবস্থা নির্ভরশীল তাদের যেকোনো এক বা একাধিক নিয়ামকের পরিবর্তন ঘটলে সাম্যাবস্থার অবস্থান সামনের দিকে বা পশ্চাৎ দিকে এমনভাবে স্থানান্তরিত হয় যাতে এসব পরিবর্তনের প্রভাব প্রশমিত হয়।”
⇒ রাসায়নিক সাম্যাবস্থার ওপর তাপমাত্রা, চাপ ও ঘনমাত্রার প্রভাব : সকল উভমুখী তাপহারী বিক্রিয়ায় তাপমাত্রা বৃদ্ধি করলে সাম্যাবস্থার অবস্থান সামনের দিকে বা ডান দিকে এবং তাপমাত্রা হ্রাস করলে তা পশ্চাৎ দিকে বা বাম দিকে স্থানান্তরিত হয়। অন্যদিকে, সকল উভমুখী তাপ উৎপাদী বিক্রিয়ায় তাপমাত্রা বৃদ্ধি করলে সাম্যাবস্থার অবস্থান পশ্চাৎ দিকে বা বাম দিকে এবং তাপমাত্রা হ্রাস করলে তা সম্মুখ দিকে বা ডানদিকে স্থানান্তরিত হয়।
কঠিন ও তরল মাধ্যমে বিক্রিয়ার ক্ষেত্রে চাপের কোনো প্রভাব নেই। যে বিক্রিয়ায় উভয় দিকে সমান সংখ্যক গ্যাসীয় অণু থাকে তাতেও চাপের কোনো প্রভাব নেই। যে বিক্রিয়ায় গ্যাসীয় অণুর সংখ্যা হ্রাস পায়, চাপ বাড়ালে ঐ বিক্রিয়া সামনের দিকে অগ্রসর হয়। বিক্রিয়ায় অণুর সংখ্যা বৃদ্ধি পেলে বা চাপ বাড়ালে বিক্রিয়া পেছনের দিকে যায়।
আর কোনো বিক্রিয়কের ঘনমাত্রা বাড়ালে বিক্রিয়া সামনের দিকে যাবে; উৎপাদের ঘনমাত্রা বাড়লে বিক্রিয়া পেছনের দিকে যাবে।
রসায়ন সপ্তম অধ্যায় রাসায়নিক বিক্রিয়া জ্ঞানমূলক প্রশ্ন ও উত্তর
প্রশ্ন \ 1 \ রেডক্স শব্দের অর্থ কী?
উত্তর : রেডক্স শব্দের অর্থ জারণ-বিজারণ।
প্রশ্ন \ 2 \ বরফের রাসায়নিক সংকেত কোনটি?
উত্তর : বরফের রাসায়নিক সংকেত H2O(s)।
প্রশ্ন \ ৩ \ এস্টার কী?
উত্তর : অ্যালকোহল ও জৈব এসিডের বিক্রিয়ায় যে যৌগ উৎপন্ন হয় তাকে এস্টার বলা হয়।
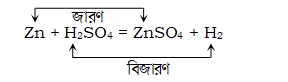
প্রশ্ন \ ৪ \ Zn + H2SO4 = ZnSO4 + H2 এটি কোন ধরনের বিক্রিয়া?
উত্তর : প্রতিস্থাপন বিক্রিয়া।
প্রশ্ন \ ৫ \ মোমের প্রধান উপাদান কী?
উত্তর : মোমের প্রধান উপাদান হলো বিভিন্ন হাইড্রোকার্বনের মিশ্রণ।
প্রশ্ন \ 6 \ জারক কীভাবে বিজারিত হয়?
উত্তর : জারক বিজারক থেকে ইলেকট্রন গ্রহণ করে বিজারিত হয়।
প্রশ্ন \ ৭ \ জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়ক ইলেকট্রন গ্রহণ করে তাকে কী বলে?
উত্তর : জারক।
প্রশ্ন \ 8 \ আমরা খাদ্য লবণ হিসেবে কী ব্যবহার করি?
উত্তর : সোডিয়াম ক্লোরাইড (NaCl)।
প্রশ্ন \ 9 \ জানালার গ্রিলে পড়া বাদামি আস্তরণের নাম কী?
উত্তর : জানালার গ্রিলে পড়া বাদামি আস্তরণের নাম মরিচা। এটি পানিযুক্ত ফেরিক অক্সাইড। এর সংকেত Fe2O3. 3H2O।
প্রশ্ন \ 1০ \ দহনের জন্য কী প্রয়োজন?
উত্তর : অক্সিজেন।
প্রশ্ন \ 11 \ রাসায়নিক বিক্রিয়ায় সমতা চিহ্নের আগের অংশকে কী বলে?
উত্তর : রাসায়নিক বিক্রিয়ায় সমতা চিহ্নের আগের অংশকে বিক্রিয়ক বলে।
প্রশ্ন \ 12 \ দুটি জারক এবং দুটি বিজারক পদার্থের নাম লেখ।
উত্তর : দুটি জারক পদার্থের নাম : O2 ও HNO3
দুটি বিজারক পদার্থের নাম : H2 ও C
প্রশ্ন \ 1৩ \ O2 নেই এমন একটি জারক পদার্থ এবং H2 নেই এমন একটি বিজারক পদার্থের নাম লেখ।
উত্তর : O2 নেই এমন একটি জারক পদার্থ Cl2 আর H2 নেই এমন একটি বিজারক পদার্থ CO।
প্রশ্ন \ 1৪ \ বিজারক হিসেবে কাজ করে এমন একটি গ্যাসের নাম লেখ।
উত্তর : বিজারক হিসেবে কাজ করে এমন একটি গ্যাস হলো NH3।
প্রশ্ন \ 1৫ \ প্রশমন বিক্রিয়া কী?
উত্তর : একটি ক্ষারক ও অ¤েøর মধ্যে বিক্রিয়ার মাধ্যমে লবণ ও পানি সৃষ্টি হওয়াকে প্রশমন বলা হয়।
প্রশ্ন \ 16 \ সমাণুকরণ বিক্রিয়া কাকে বলে?
উত্তর : যে বিক্রিয়ায় কোনো যৌগের অণুতে পরমাণুসমূহ পুনর্বিন্যস্ত হয়ে অন্য সমাণু উৎপন্ন করে তাকে সমাণুকরণ বিক্রিয়া বলা হয়।
প্রশ্ন \ 1৭ \ NaCl(aq) + AgNO3(aq) → NaNO3(aq) + AgCl(s) বিক্রিয়াটি কোন ধরনের?
উত্তর : অধঃক্ষেপণ বিক্রিয়া।
প্রশ্ন \ 18 \ জলীয়বাষ্প কীভাবে উৎপন্ন হয়?
উত্তর : পানিকে 1০০0C তাপমাত্রায় উত্তপ্ত করলে জলীয়বাষ্প উৎপন্ন হয়।
প্রশ্ন \ 19 \ মোমের প্রধান উপাদান কোনটি?
উত্তর : মোমের প্রধান উপাদান বিভিন্ন হাইড্রোকার্বনের মিশ্রণ।
প্রশ্ন \ 2০ \ রাসায়নিক বিক্রিয়া কীভাবে সম্পন্ন হয়?
উত্তর : পদার্থে বিদ্যমান পরমাণুসমূহের মধ্যবর্তী বন্ধন ভাঙা এবং নতুন বন্ধন গঠনের মাধ্যমে রাসায়নিক বিক্রিয়া সম্পন্ন হয়।
প্রশ্ন \ 21 \ রাসায়নিক বন্ধন কী?
উত্তর : রাসায়নিক বন্ধন মূলত এক প্রকার শক্তি।
প্রশ্ন \ 22 \ সম্মুখমুখী বিক্রিয়া কাকে বলে?
উত্তর : যে বিক্রিয়ায় বিক্রিয়কসমূহ বিক্রিয়া করে উৎপাদে পরিণত হয়, তাকে সম্মুখমুখী বিক্রিয়া বলে।
প্রশ্ন \ 23 \ ধনাত্মক জারণ সংখ্যা কী?
উত্তর : ইলেকট্রন বর্জন করে ধনাত্মক আয়নে পরিণত হলে মৌলের জারণ সংখ্যাকে ধনাত্মক জারণ সংখ্যা বলে।
প্রশ্ন \ 24 \ ঋণাত্মক জারণ সংখ্যা কী?
উত্তর : ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে পরিণত হলে মৌলের জারণ সংখ্যাকে ঋণাত্মক জারণ সংখ্যা বলে।
প্রশ্ন \ 25 \ মৌলের জারণ সংখ্যা মূলত কিসের সাথে সম্পর্কিত?
উত্তর : মৌলের জারণ সংখ্যা মূলত তার ইলেকট্রন বিন্যাসের সাথে সম্পর্কিত।
প্রশ্ন \ 26 \ প্রতিস্থাপন বিক্রিয়া কী?
উত্তর : কোনো যৌগের একটি মৌল বা যৌMgূলককে অপর কোনো মৌল বা যৌMgূলক দ্বারা প্রতিস্থাপন করে নতুন যৌগ উৎপন্ন করার প্রক্রিয়ার নাম প্রস্থিাপন বিক্রিয়া।
প্রশ্ন \ 27 \ অ্যালডিহাইডের জারণে কী উৎপন্ন হয়?
উত্তর : অ্যালডিহাইডের জারণে জৈব এসিড উৎপন্ন হয়।
রসায়ন সপ্তম অধ্যায় রাসায়নিক বিক্রিয়া অনুধাবনমূলক প্রশ্ন ও উত্তর
প্রশ্ন \ 1 \ আর্দ্রবিশ্লেষণ বিক্রিয়া বলতে কী বোঝায়?
উত্তর : যে দ্বিবিযোজন বিক্রিয়ায় পানি কোনো যৌগের সঙ্গে বিক্রিয়া করে এক বা একাধিক নতুন যৌগ উৎপাদন করে, তাকে আর্দ্রবিশ্লেষণ বা পানিযোজন বিক্রিয়া বলা হয়। যেমন : এস্টারের আর্দ্রবিশ্লেষণে এসিড ও অ্যালকোহল উৎপাদিত হয়।
CH3COOCH2CH3 + H2O = CH3COOH + CH3CH2OH
প্রশ্ন \ 2 \ MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O-এ বিক্রিয়ায় কোনটি জারক এবং কোনটি বিজারক তা লেখ।
উত্তর : MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O- এ বিক্রিয়ায় MnO2 জারক এবং HCl বিজারক।
প্রশ্ন \ 3 \ PbS + 4H2O2 = PbSO4 + 4H2O-এ বিক্রিয়ায় কোনটি জারিত হচ্ছে এবং কোনটি বিজারিত হচ্ছে?
উত্তর : PbS এর সঙ্গে H2O2 বিক্রিয়া ঘটালে PbS জারিত হয়ে সাদা রঙের PbSO4 উৎপন্ন করে; আর H2O2 নিজে বিজারিত হয়ে H2O-তে পরিণত হয়।
প্রশ্ন \ 4 \ ফেরাস ক্লোরাইডের সাথে ক্লোরিনের বিক্রিয়ায় ফেরিক ক্লোরাইড উৎপন্ন হয়। এটি কী ধরনের বিক্রিয়া?
উত্তর : ফেরাস ক্লোরাইডের সাথে ক্লোরিনের বিক্রিয়ায় ফেরিক ক্লোরাইড উৎপন্ন হয়।
2FeCl2 + Cl2 → 2FeCl3
এক্ষেত্রে বিক্রিয়কে আয়রনের যোজনী 2।কিন্তু উৎপাদে আয়রনের যোজনী 3। বিক্রিয়ার ফলে আয়রনের যোজনী বৃদ্ধি পেয়েছে। আবার বিক্রিয়কে ক্লোরিনের যোজনী শূন্য এবং উৎপাদে ক্লোরিনের যোজনী 1। এক্ষেত্রেও ক্লোরিনের যোজনী বৃদ্ধি পেয়েছে। সুতরাং বিক্রিয়াটি একটি জারণ-বিজারণ বিক্রিয়া।
প্রশ্ন \ 5 \ নিচের পদার্থগুলোর কোনটি জারক এবং কোনটি বিজারক তা লেখ :
HNO3, CO, SO2, NH3, H2S, H2SO4, Cl2, KMnO4
উত্তর : উল্লিখিত পদার্থগুলোর মধ্যে জারক পদার্থ : HNO3, H2SO4, Cl2, KMnO4 আর বিজারক পদার্থ : CO, SO2, NH3, H2S।
প্রশ্ন \ 6 \ প্লাস্টিক প্রস্তুতিতে পলিমারকরণ বিক্রিয়ার ভ‚মিকা কী?
উত্তর: পলিমারকরণ বিক্রিয়ায় এক বা একাধিক যৌগের অনেকগুলো অণু পরস্পরের সঙ্গে যুক্ত হয়ে বড় অণু সৃষ্টি করে। পলিইথিলিন হচ্ছে প্লাস্টিক। এ বিক্রিয়ায় ইথিলিনের বহুসংখ্যক অণু একত্রিত হয়ে পলিইথিলিন তৈরি করে।
nCH2 = CH2 (- CH2 – CH2- )n
প্রশ্ন \ 7 \ চুনে পানি যোগ করা হলে কোন ধরনের বিক্রিয়া হবে?
উত্তর : চুন হলো ক্যালসিয়াম অক্সাইড। চুনে পানি যোগ করা হলে প্রচুর তাপ উৎপন্ন হয় এবং চুন ফুলে ওঠে। চুনের সঙ্গে পানির রাসায়নিক বিক্রিয়ায় কলিচুন বা ক্যালসিয়াম হাইড্রোক্সাইড উৎপন্ন হয়। এটি একটি তাপ উৎপাদী বিক্রিয়া।
CaO + H2O –→ Ca(OH)2 + তাপ
ক্যালসিয়াম ক্যালসিয়াম হাইড্রোক্সাইড
প্রশ্ন \ 8 \ নিম্নলিখিত বিক্রিয়াগুলো কোনটি কোন শ্রেণির?
i. CaO + CO2 = CaCO3
ii. 2KClO3 = 2KCl + 3O2
iii. NH4CNO –→ H2N – CO – NH2
উত্তর :
i. CaO + CO2 = CaCO3
এটি একটি সংযোজন বিক্রিয়া। কারণ, CaO ও CO2 এর প্রত্যক্ষ সংযোগে CaCO3 উৎপন্ন হয়।
ii. 2KClO3 = 2KCl + 3O2
এটি একটি বিযোজন বিক্রিয়া। কারণ, KClO3 যৌগের উপাদানসমূহ বিভক্ত হয়ে KCl ও O2 উৎপন্ন করে।
iii. NH4CNO → H2N – CO – NH2
এটি একটি সমাণুকরণ বিক্রিয়া। কারণ, NH4CNO যৌগের অণুতে বিদ্যমান পরমাণুসমূহ পুনর্বিন্যস্ত হয়ে H2N – CO – NH2 উৎপন্ন হয়েছে।
প্রশ্ন \ 9 \ দেখাও যে, H2S বিজারকরূপে কাজ করে।
উত্তর : Cl2 পানির মধ্যে H2S গ্যাস চালনা করলে Cl2 বিজারিত হয়ে HCl-এ পরিণত হয়, আর H2S জারিত হয়ে হলুদ বর্ণের S উৎপন্ন করে। এখানে Cl2 জারক এবং H2S বিজারক।
H2S + Cl2 = 2HCl + S
প্রশ্ন \ 1০ \ সকল সংশ্লেষণ বিক্রিয়াই সংযোজন বিক্রিয়া তবে সকল সংযোজন বিক্রিয়া সংশ্লেষণ বিক্রিয়া নয়- ব্যাখ্যা কর।
উত্তর : যে রাসায়নিক বিক্রিয়ায় দুই বা ততোধিক মৌলিক বা যৌগিক পদার্থ পরস্পর বিক্রিয়া করে একটি মাত্র যৌগ উৎপন্ন করে তাকে সংযোজন বিক্রিয়া বলে। আর যে সংযোজন বিক্রিয়ায় দুই বা ততোধিক মৌলিক পদার্থ যুক্ত হয়ে একটি মাত্র যৌগ উৎপন্ন করে তাকে সংশ্লেষণ বিক্রিয়া বলে। যেমন :
i. NH3 + HCl –→ NH4Cl
ii. 2H2 + O2 2H2O
iii. ঈ + O2 CO2
উপরের তিনটি বিক্রিয়াই সংযোজন বিক্রিয়া। এর মধ্যে (ii) ও (iii) নং বিক্রিয়ায় শুধু মৌলিক পদার্থ যুক্ত হয়ে একটি যৌগ গঠন করায় এ দুটি বিক্রিয়াকে সংশ্লেষণ বিক্রিয়া বলা হয়। সুতরাং, সকল সংশ্লেষণ বিক্রিয়াই সংযোজন বিক্রিয়া তবে সকল সংযোজন বিক্রিয়া সংশ্লেষণ বিক্রিয়া নয়।
প্রশ্ন \ 11 \ Zn + H2SO4 = ZnSO4 + H2-এ বিক্রিয়াটিকে কি জারণ-বিজারণ বিক্রিয়া বলা হয়, কেন?
উত্তর : Zn + H2SO4 = ZnSO4 + H2-এ বিক্রিয়াটিকে জারণ-বিজারণ বিক্রিয়া বলা যায়। এখানে তড়িৎ ধনাত্মক Zn এর সঙ্গে তড়িৎ ঋণাত্মক মূলক SO4 যুক্ত হয়ে ZnSO4 উৎপন্ন করে। ফলে Zn জারিত হয় অর্থাৎ Zn বিজারক। আবার, H2SO4 থেকে তড়িৎ ঋণাত্মক SO4 অপসারিত হয়ে H2 উৎপন্ন হয়। ফলে H2SO4 বিজারিত হয়। এখানে লঘু H2SO4 জারক হিসেবে কাজ করে।
প্রশ্ন \ 12 \ নিচের সমীকরণগুলো সমতা বিধান করে সম্পূর্ণ কর।
ক. N2 + H2 =
খ. MgO + HCl =
গ. CaCO3 + HCl =
ঘ. Na2CO3 + CaCl2 =
ঙ. FeCl3 + H2O =
চ. NH4OH + HCl =
উত্তর :
ক. N2 + 3H2 = 2NH3
খ. MgO + 2HCl = MgCl2 + H2O
গ. CaCO3 + 2HCl = CaCl2 + CO2 + H2O
ঘ. Na2CO3 + CaCl2 = 2NaCl + CaCO3
ঙ. 2FeCl3 + 3H2O = Fe2O3 + 6HCl
চ. NH4OH + HCl = NH4Cl + H2O
প্রশ্ন \ 1৩ \ সংযোজন ও সংশ্লেষণ বিক্রিয়ার মধ্যে পার্থক্য কী?
উত্তর : সংযোজন ও সংশ্লেষণ বিক্রিয়ার মধ্যে পার্থক্য :
| সংযোজন বিক্রিয়া | সংশ্লেষণ বিক্রিয়া |
| 1। যে রাসায়নিক বিক্রিয়ায় কোন যৌগ এর সরলতম উপাদানসমূহের প্রত্যক্ষ সংযোগে সৃষ্টি হয় তাকে সংযোজন বিক্রিয়া বলে। যেমন :
2H2 + O2 = 2H2O C + O2 = CO2 NH3 + HCl = NH4Cl |
1। যে রাসায়নিক বিক্রিয়ায় কোনো যৌগ এর উপাদান মৌলসমূহের প্রত্যক্ষ সংযোগের ফলে সৃষ্টি হয় তাকে সংশ্লেষণ বিক্রিয়া বলে। যেমন :
2H2 + O2 = 2H2O 3H2 + N2 = 2NH3 |
| 2। সকল সংযোজন বিক্রিয়া সংশ্লেষণ বিক্রিয়া নয়। | 2। সকল সংশ্লেষণ বিক্রিয়াই সংযোজন বিক্রিয়া। |
প্রশ্ন \ 1৪ \ মোমবাতি দহনে ভৌত এবং রাসায়নিক পরিবর্তন একসাথে ঘটে ব্যাখ্যা কর।
উত্তর : একটি মোমবাতি যখন জ্বলে তখন মোমের মধ্যস্থ C এবং H2 বায়ুর O2-এর সাথে রাসায়নিক বিক্রিয়া করে CO2 এবং H2O তে পরিণত হয়- এটি হলো মোমের রাসায়নিক পরিবর্তন। এ পরিবর্তনে যে তাপ উৎপন্ন হয় তার দ্বারা কিছু পরিমাণ মোম গলে তরল হয়- এটি হলো মোমের ভৌত পরিবর্তন। সুতরাং, একটি মোমবাতির দহনে ভৌত এবং রাসায়নিক পরিবর্তন একসাথে ঘটে।
প্রশ্ন \ 1৫ \ রাসায়নিক পরিবর্তনের বৈশিষ্ট্য লেখ।
উত্তর : রাসায়নিক পরিবর্তনের বৈশিষ্ট্য :
i. রাসায়নিক পরিবর্তন স্থায়ী। পরিবর্তিত পদার্থকে সহজে মূল পদার্থে ফিরিয়ে আনা যায় না। কারণ মূল পদার্থ এবং রাসায়নিক পরিবর্তনের পর প্রাপ্ত পদার্থের মধ্যে অণুর গঠনের আমূল পরিবর্তন হয়।
iii. রাসায়নিক পরিবর্তনে তাপের পরিবর্তন অবশ্যম্ভাবী। যেকোনো রাসায়নিক পরিবর্তনে তাপ উৎপন্ন হয় অথবা শোষিত হয়।
প্রশ্ন \ 16 \ রাসায়নিক সাম্যাবস্থাকে গতিময় অবস্থা বলা হয় কেন?
উত্তর : রাসায়নিক সাম্যাবস্থায় একই সাথে সম্মুখ ও পশ্চাৎ দুই বিক্রিয়াই সংঘটিত হয়। তবে এই অবস্থায় সম্মুখ বিক্রিয়া যে হারে ঘটে পশ্চাৎ বিক্রিয়া একই হারে ঘটে। তাই আপাতদৃষ্টিতে দেখলে মনে হয় এটি একটি স্থির অবস্থ্ াকিন্তু প্রকৃতপক্ষে এটি একটি গতিময় অবস্থা। তাই রাসায়নিক সাম্যাবস্থাকে গতিময় অবস্থা বলা হয়।
প্রশ্ন \ 1৭ \ এন্টাসিড জাতীয় ঔষধ সেবনে কোন ধরনের বিক্রিয়া ঘটে?
উত্তর : এন্টাসিড জাতীয় ঔষধ সেবনে প্রশমন বিক্রিয়া সম্পন্ন হয়। কারণ এন্টাসিড জাতীয় ঔষধে ধাতব হাইড্রোক্সাইড [যেমন : Al(OH)3; Mg(OH2)] থাকে যা ক্ষারধর্মী। এটি পাকস্থলির হাইড্রোক্লোরিক এসিড (HCl) এর সাথে বিক্রিয়া করে নিরপেক্ষ লবণ ও পানি উৎপন্ন করে। ফলে পেটের জ্বালা যন্ত্রণা দূর হয়, বিক্রিয়াটি নিম্নরূপ :
3HCl + Al(OH)3 → AlCl3 + 3H2O
প্রশ্ন \ 18 \ জারণ সংখ্যা ও যোজনী এক নয় কেন?
উত্তর : জারণ সংখ্যা হলো এমন একটি সংখ্যা, যা দ্বারা মৌলের পরমাণুতে সৃষ্ট তড়িৎ চার্জের প্রকৃতি ও সংখ্যামান উভয়ই প্রকাশ পায়।
অপরদিকে যোজনী হলো একটি মৌল অপর মৌলের সাথে যুক্ত হওয়ার ক্ষমতা। তাছাড়া জারণ সংখ্যা ধনাত্মক ও ঋণাত্মক হতে পারে, স্থির যোজনী একটি পূর্ণ সংখ্যা। এ কারণেই জারণ সংখ্যা ও যোজনী এক নয়।